Este enlace se produce como consecuencia de la compartición de los electrones de los elementos que se enlazan, es decir, no existe una cesión de electrones sino que éstos quedan asociados conjuntamente a los dos elementos (entre el enlace iónico puro y el enlace covalente puro existe un enlace mixto iónico-covalente de mayor o menor carácter iónico, en el que los electrones compartidos, en cierta forma, están asociados más a uno de los elementos).
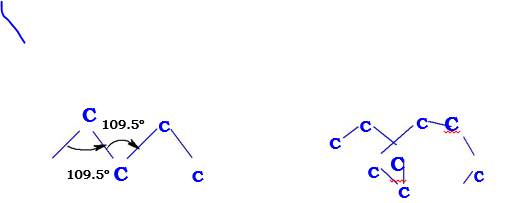
La característica fundamental del enlace es su direccionalidad. Así por ejemplo, el carbono presenta cuatro electrones de valencia que pueden dar lugar a cuatro enlaces que forman entre ellos 109.5º; esto puede provocar, en el caso de grandes cadenas moleculares, macromoléculas o polímeros, materiales tales como los elastómeros, en los que al aplicar pequeñas fuerzas pueden estirarse o alargarse en forma muy considerable, incluso varias veces su longitud inicial sin romperse.
En el caso del carbono, éste se enlaza convalentemente consigo mismo pudiendo formar moléculas con varios miles de enlaces entre carbonos, constituyendo lo que se conoce como polímeros. Estos enlaces se representan mediante un pequeño guión entre los elementos que se enlazan (C-C) y como el enlace corresponde a dos electrones compartidos se puede representar por dos puntos (C:C)
El carbono, con cuatro electrones de valencia, puede combinarse covalentemente mediante cuatro enlaces, tal y como se representa en la figura.
Por ejemplo, el metano, CH4. También puede combinarse utilizando dobles o triples enlaces entre elementos y, es frecuente, que esos dobles enlaces surjan entre átomos de carbono enlazados tal y como ocurre con la molécula de etileno (CH2=CH2).
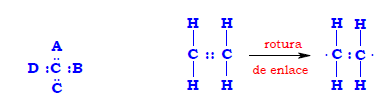
Si por alguna razón se rompe alguno de los enlaces de una molécula de etileno, queda un compuesto en el que los carbonos están enlazados por un enlace simple y disponen cada uno de ellos de un electrón de valencia que les permite enlazarse con otros elementos o compuestos.
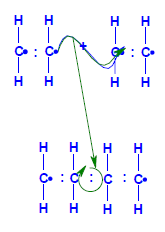
Si dos moléculas de etileno en las que se ha roto uno de los enlaces se combinan mediante los electrones de valencia se forma una cadena con cuatro átomos de carbono con dos electrones de valencia en sus extremos que les permite seguir combinándose con nuevas moléculas de etileno, dando lugar a cadenas en las que puede haber miles de eslabones como el que aparece en la figura produciéndose lo que se conoce como polietileno.
![]()
En los elastómeros, como los enlaces covalentes no son lineales, las macromoléculas pueden no presentar una dirección preferente de los enlaces, dando lugar a un posible arrollamiento similar a un rizo, de forma que cuando se aplica un estiramiento, esta molécula se orienta en la dirección de la fuerza sin necesidad de alterar los enlaces.
Fuente: Apuntes de Ciencia de Materiales. Ingeniería Química – Universidad de Huelva