La cúbica centrada α= en β = el γ interior corresponde a una red cúbica, por lo tanto a = b = c y α = 90º, en la que las partículas se encuentran en los vértices y una en el centro del cubo.
Cada átomo de los vértices se encuentra compartido por ocho celdas y por tanto sólo un octavo de átomo de cada vértice se encuentra en el interior de cada celda.

Esto se conoce como número de átomos propios de la red.
Se define el factor de empaquetamiento como la relación entre el volumen realmente ocupado por los átomos considerados bolas rígidas y el volumen del cristal.
En el caso de la estructura cúbica centrada, el factor de empaquetamiento se puede determinar de la siguiente forma:
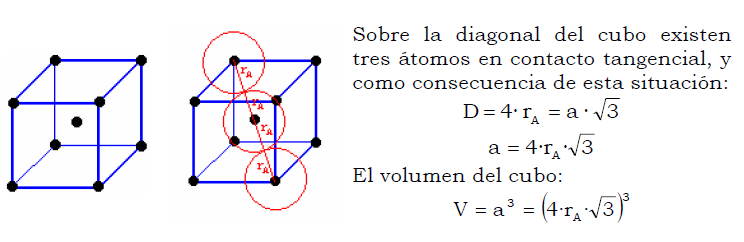
Volumen en el que se está considerando tanto la parte ocupada por los átomos como los huecos entre ellos, es decir, todo el cubo.
El volumen real ocupado por los átomos es el volumen de 1 átomo multiplicado por el número de átomos en el interior del cubo:
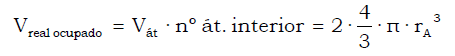
Fuente: Apuntes de Ciencia de Materiales. Ingeniería Química – Universidad de Huelva