 El hecho de que muchas propiedades de los elementos variasen periódicamente indujo a los químicos a buscar una clasificación de los elementos en función de sus analogías. Un primer intento de clasificación se debe al químico alemán Döbereiner (1780-1849) que observó la existencia de grupos de tres elementos, a los que denominó tríadas, con propiedades análogas y en las cuales se cumplía que el peso atómico del elemento central era aproximadamente el promedio de los elementos de los extremos de la tríada.
El hecho de que muchas propiedades de los elementos variasen periódicamente indujo a los químicos a buscar una clasificación de los elementos en función de sus analogías. Un primer intento de clasificación se debe al químico alemán Döbereiner (1780-1849) que observó la existencia de grupos de tres elementos, a los que denominó tríadas, con propiedades análogas y en las cuales se cumplía que el peso atómico del elemento central era aproximadamente el promedio de los elementos de los extremos de la tríada.
Así, por ejemplo, Li, Na y K o bien CI, Br y I.
En 1864 el químico inglés Newlands (1837-1898) ordenó los elementos en orden de pesos atómicos crecientes y observó que el octavo elemento a partir de uno cualquiera tenía propiedades análogas a él.
No obstante, su ordenación por «octavas» no podía aplicarse más allá del calcio debido a la aparición de los elementos de transición.
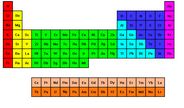
La solución la encontraron en 1869, trabajando independientemente, el químico ruso Mendeleiev (1834-1907) y el químico alemán Lothar Meyer (1830-1895), que construyeron una tabla periódica ordenando los elementos en orden de pesos atómicos crecientes, pero respetando las analogías entre sus propiedades, no dudando en dejar lugares vacíos en la tabla para elementos desconocidos en la época o en invertir la posición de algunos elementos en función de sus analogías químicas.
La ordenación definitiva la encontró el químico inglés Moseley (1887-1915), quien en 1913 descubrió, a partir de sus investigaciones sobre los espectros de rayos X de los elementos, que la ordenación correcta de los elementos se establecía en base a sus números atómicos.